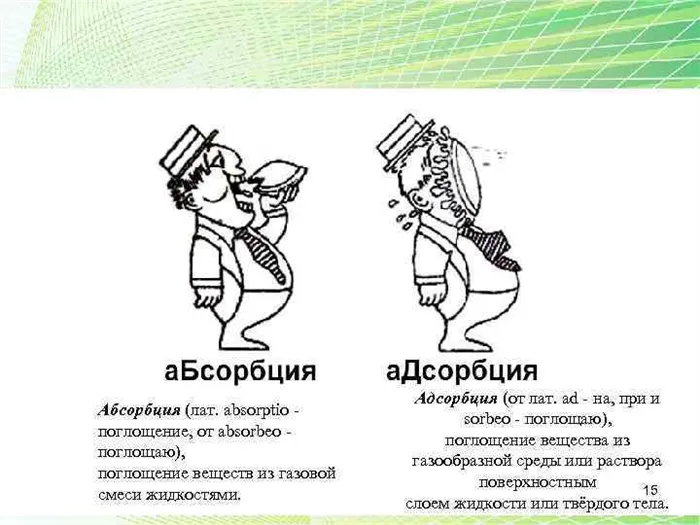
Механизм
Механизм адсорбции основан на притяжении между адсорбентом и адсорбатом. Это притяжение может быть химическим или физическим по своей природе. Химическая адсорбция происходит, когда происходят химические реакции между адсорбентом и адсорбатом, образуя химические связи и образцы. Физическая адсорбция основана на ослабленных притяжениях, таких как ван-дер-ваальсовы силы или притяжение диполя. Механизм адсорбции может варьироваться в зависимости от типа адсорбента и адсорбата.
Абсорбция, с другой стороны, основана на диффузии. Когда абсорбат взаимодействует с абсорбентом, он проникает в структуру абсорбента, распространяясь внутри него. Механизм абсорбции может включать физическую или химическую абсорбцию. Физическая абсорбция происходит с использованием слабых физических сил, таких как ван-дер-ваальсовы силы или силы поверхностного натяжения. Химическая абсорбция включает в себя химическую реакцию между абсорбирующим веществом и абсорбируемым веществом.
Адсорбция
Основным механизмом адсорбции является притяжение между частицами адсорбента и адсорбата. Это может происходить за счет различных физико-химических сил, таких как ван-дер-ваальсовы силы, ковалентные связи или электростатические взаимодействия.
Адсорбция может происходить на различных поверхностях, включая твердые тела, жидкости и газы. Например, в промышленности адсорбция широко используется для очистки газов и жидкостей от загрязнений, а также для обработки поверхностей материалов.
Одним из примеров адсорбции является явление адсорбции газов на поверхности твердого вещества. Это может быть полезно, например, для очистки воздуха от вредных веществ или для хранения газов в высоких концентрациях.
Одной из особенностей адсорбции является то, что процесс обратимый. То есть адсорбаты могут легко взаимодействовать с адсорбентом, а затем освобождаться обратно в среду.
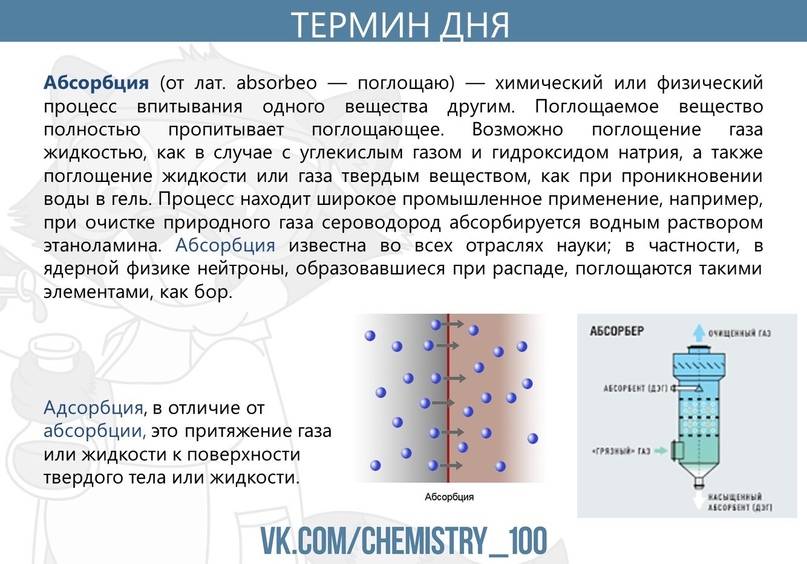
Важно отличать адсорбцию от абсорбции. Абсорбция – это процесс, при котором одно вещество проникает в объем другого вещества
Таким образом, в отличие от адсорбции, абсорбция происходит не только на поверхности, но и внутри адсорбента.
В целом, адсорбция – это важное явление, которое широко применяется в различных областях науки и промышленности. Понимание процесса адсорбции позволяет разработать эффективные методы очистки веществ и улучшить работу различных систем
Что такое адсорбция и где она применяется?
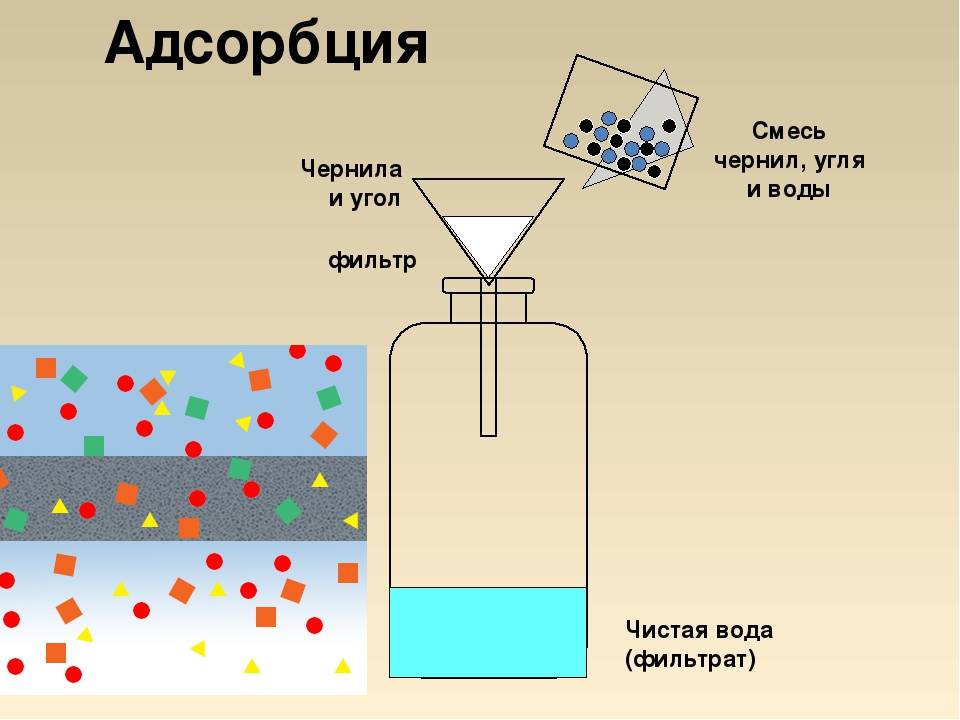
На практике адсорбция широко используется для концентрирования веществ, очистки газов и жидкостей от примесей. Адсорбционные методы анализа применяются для определения удельной поверхности твердых веществ, оценки размера А нанесенных частиц (в том числе наноразмерных) на поверхности носителя и т.
Что такое абсорбция препарата?
В медицине – физиологический процесс всасывания, то есть проникновения лекарственных веществ и ксенобиотиков через клеточные мембраны в кровь и лимфу.
Что значит абсорбировать?
АБСОРБИРОВАТЬ — (от лат. absorbere всасывать поглощать). В физиологии действие, по которому лимфатические и млечные сосуды несут питательные материалы внутрь живого существа, удерживают их здесь, принимают и извергают негодные для тела вещества и, таким образом … Словарь иностранных слов русского языка
Что такое абсорбция в электротехнике?
Коэффициент абсорбции в электротехнике — это отношение измеренного мегаомметром значения сопротивления изоляции на 60-ти секундах к измеренному на 15-ти. Чем больше геометрические размеры и лучше качество изоляции, препятствующей этому, тем больше требуется времени для проникновения тока в изоляцию.
Что такое абсорбирующее вещество?
абсорбция — Избирательное поглощение вещества из раствора, или газовой смеси жидкостью или твердым телом в объеме. Примечание Абсорбирующее вещество называется абсорбентом.
Что означает слово секреция?
Секре́ция — это процесс выделения химических соединений из клетки . В отличие от собственно выделения, при секреции у вещества может быть определённая функция . Секрет — жидкость , выделяемая клетками и содержащая биологически активные вещества. Органы, выделяющие секрет, называются железами .
Что такое секреция в биологии?
Секре́ция — процесс выделения химических соединений из клетки. В отличие от собственно выделения, при секреции у вещества может быть определённая функция (оно может не быть отходами жизнедеятельности). Секрет — жидкость, выделяемая клетками и содержащая биологически активные вещества.
Что является железой внутренней секреции?
Эндокринные железы (железы внутренней секреции) — железы и параганглии, синтезирующие гормоны, которые выделяются в кровеносные (венозные) или лимфатические капилляры.
Механизмы и характеристики химической сорбции
Химическая сорбция представляет собой процесс адсорбции, при котором поглощаемые вещества взаимодействуют с поверхностью адсорбента, образуя химические связи. Этот механизм отличается от физической сорбции, при которой поглощаемые вещества просто адсорбируются на поверхности без образования химических связей.
При химической сорбции взаимодействие между поглощаемым веществом и поверхностью адсорбента осуществляется по принципу химической реакции, в результате которой образуются новые химические связи. Эти связи могут быть ковалентными или ионными, в зависимости от природы поглощаемых веществ и поверхности адсорбента.
Характеристики химической сорбции включают следующие элементы:
Селективность: некоторые адсорбенты могут предпочитать поглощать некоторые вещества из смеси, основываясь на их химической природе. Это позволяет использовать химическую сорбцию для селективной очистки или разделения смесей.
Емкость: характеризует способность адсорбента удерживать поглощаемое вещество на своей поверхности. Чем выше емкость, тем больше вещества может быть поглощено.
Кинетика: описывает скорость процесса химической сорбции. Изучение кинетики позволяет определить оптимальные условия для проведения процесса.
Равновесие: достигается, когда скорость адсорбции равна скорости десорбции, то есть поглощаемые и выделяемые вещества находятся в равновесии
Установление равновесия важно для определения емкости адсорбента и его эффективности.
Химическая сорбция является одним из важных процессов в различных областях, включая промышленность, экологию и медицину. На основе понимания механизмов и характеристик химической сорбции можно разрабатывать новые методы и технологии для улучшения процессов поглощения веществ и применения их в практике.
Физический процесс
Адсорбция является процессом, при котором молекулы или ионы одного вещества (адсорбата) прилипают к поверхности другого вещества (адсорбента). Во время адсорбции, адсорбат остается на поверхности адсорбента, образуя адсорбционную оболочку или мономолекулярный слой. Этот процесс происходит преимущественно на поверхностях твердых тел или жидкостей.
Абсорбция, с другой стороны, представляет собой процесс поглощения одного вещества другим веществом. Для абсорбции свойственно проникновение абсорбата внутрь абсорбента. В отличие от адсорбции, абсорбция может происходить как в твердых телах, так и в жидкостях.
Одним из ключевых отличий между адсорбцией и абсорбцией является механизм взаимодействия. Во время адсорбции, происходит притяжение адсорбата к поверхности адсорбента на основе различных физических сил, таких как ван-дер-ваальсовы силы или химические связи. В случае абсорбции, абсорбат проникает внутрь абсорбента благодаря различным процессам диффузии.
Использование адсорбции и абсорбции имеет широкий спектр применения в различных областях. Например, процесс адсорбции используется в каталитических процессах, фильтрации и очистке воздуха и воды. Абсорбция, с другой стороны, находит применение в различных химических процессах, таких как абсорбция газов или абсорбция ионов.
Адсорбция
Процесс адсорбции происходит в результате взаимодействия между адсорбентом (поверхностью твердого или жидкого тела) и адсорбатом (атомами, ионами или молекулами, которые поглощаются). Адсорбат может быть поглощен внутри пор или на поверхности адсорбента.
Основное отличие адсорбции от абсорбции заключается в том, что адсорбция происходит на поверхности твердого или жидкого тела, а абсорбция — внутри материала. В процессе абсорбции адсорбат проникает внутрь материала, покидая поверхность и насыщая объем материала. В отличие от этого, в процессе адсорбции адсорбат существует только на поверхности адсорбента.
Процесс адсорбции может быть обратимым или необратимым. Обратимая адсорбция означает, что адсорбат может поглощаться и высвобождаться адсорбентом. В случае необратимой адсорбции адсорбат поглощается и остается навсегда на поверхности адсорбента.
Понимание адсорбции играет важную роль в различных областях науки и технологии. Изучение кинетики и термодинамики адсорбции позволяет оптимизировать процессы, связанные с разработкой новых материалов, улучшением сорбентов и разработкой методов очистки воды и газов от загрязнителей. Улучшение и эффективное использование процессов адсорбции имеет широкие применения в промышленности, медицине и окружающей среде.
| Преимущества адсорбции | Недостатки адсорбции |
|---|---|
| Высокая специфичность адсорбции позволяет селективно удалять определенные загрязнители из растворов или газов | Необходимость регенерации адсорбента после насыщения |
| Возможность эффективной очистки воды и газов с высокой эффективностью | Необходимость использования значительных количеств адсорбента |
| Возможность использования адсорбционных процессов для разработки новых материалов | Возможность развития необратимой адсорбции |
Абсорбция
Абсорбция может происходить как в газообразной, так и в жидкой фазе. В газообразной фазе абсорбцию можно наблюдать, например, когда газ поглощается жидкостью. В жидкой фазе абсорбцию можно наблюдать, например, когда раствор поглощает вещество.
Основными факторами, влияющими на процесс абсорбции, являются температура, давление, концентрация абсорбата и абсорбента. Величина абсорбции может быть описана различными кинетическими и термодинамическими моделями, которые учитывают эти факторы.
Абсорбция широко используется в различных областях, включая химическую промышленность, фармацевтику, пищевую промышленность, окружающую среду и др. Процессы абсорбции используются для очистки газовых и жидких потоков от различных загрязнений, а также для разделения смесей веществ.
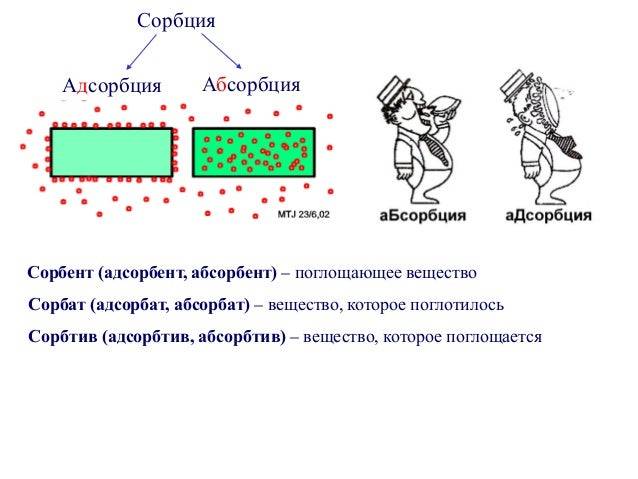
Сорбция — процесс поглощения вещества
Сорбция представляет собой физический процесс, при котором вещества поглощаются или адсорбируются из основной среды (газа или жидкости) на поверхности другого вещества — сорбента. Во время сорбции происходит проникновение молекул адсорбата в структуру сорбента, что позволяет удерживать и концентрировать вещество.
Сорбция может происходить по различным механизмам, включая физическую адсорбцию и хемосорбцию. В случае физической адсорбции молекулы адсорбата слабо связаны с поверхностью сорбента и могут быть отделены при изменении условий (например, понижение температуры или повышение давления). Хемосорбция, напротив, является более прочным и химическим процессом, при котором молекулы адсорбата взаимодействуют с поверхностью сорбента через химические связи.
Сорбция широко используется в различных областях, включая промышленность, медицину и окружающую среду. К примеру, в промышленности сорбция применяется для очистки газов и жидкостей от различных примесей, а также для разделения смесей веществ. В медицине сорбция используется для обнаружения и извлечения лекарственных веществ из организма. В области охраны окружающей среды сорбция применяется для улавливания и удаления загрязнителей из воды и воздуха.
Важным аспектом сорбции является выбор оптимального сорбента для конкретных задач. Подходящий сорбент должен обладать высокой сорбционной емкостью, способностью к быстрому и эффективному поглощению вещества, а также легко разделяться от адсорбата для его последующего использования или утилизации.
Абсорбционная очистка газов
Абсорбционный метод очистки газов чаще всего используется в тех сферах, на которых происходит большой выброс всевозможных вредных веществ и пыли в воздух.
Абсорбер для очистки газов — устройство, в котором происходит поглощение примесей газовых компонентов жидкой фазой.
Широкое применения абсорберы получили благодаря своей высокой эффективности.
Самым популярным абсорбером является скруббер. Выделяют несколько типов скрубберов:
Подбирать тип скруббера может только специалист. В противном случае вы можете получить абсолютно неработающую установку, просто потому что неправильно подобрали абсорбент, например.
Разница в механизме взаимодействия
Абсорбция – это процесс, в котором вещество впитывает молекулы другого вещества в свою структуру. При абсорбции молекулы вещества проникают внутрь материала, распределаясь по его объему. Например, при поглощении газа в жидкость, молекулы газа растворяются в молекулах жидкости и равномерно распределяются в ее объеме.
В отличие от абсорбции, адсорбция – это процесс, при котором молекулы одного вещества прилипают к поверхности другого вещества. При адсорбции молекулы адсорбента (поверхности, на которой происходит адсорбция) образуют силы притяжения с молекулами адсорбата (вещества, которое прилипает к поверхности). Таким образом, адсорбат остается на поверхности адсорбента, без проникновения в его объем.
Это значительное различие в механизме взаимодействия делает абсорбцию более эффективным процессом по сравнению с адсорбцией. При абсорбции вещество может впитывать и задерживать гораздо большее количество другого вещества. Однако, адсорбция может быть полезна в случаях, когда требуется выделить или удалить определенное вещество из смеси.
Виды адсорбции
Адсорбирование – это поверхностный процесс. Возможен он на границе двух субстанций. В зависимости от того, какое взаимодействие сорбента и сорбата, выделяют несколько видов:
физическая;
химическая;
активированная.
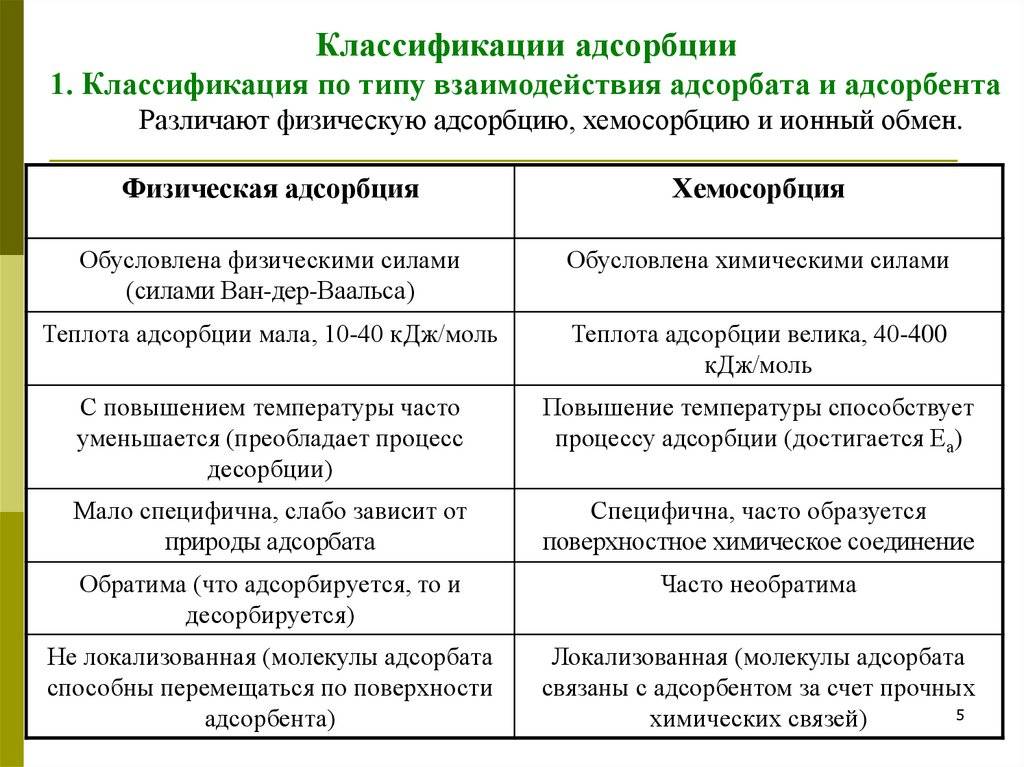
Физическая адсорбция
Это слабый и обратимый вид сорбции, при котором происходит физическое притяжении между сорбентом и сорбатом.
Процесс обусловлен Ван-Дер-Ваальсовыми силами. Они могут быть трех видов: дисперсионными, ориентационными и индукционными. Чаще всего силы являются дисперсионными. Во время взаимодействия сорбат и поверхность сорбента поляризуются, происходит выделение теплоты. Тепла при этой реакции выделяется мало, приблизительно 10 – 30 кДж/моль. При этом количество выделяемого тепла зависит от площади взаимодействия между сорбатом и сорбентом.
Также стоит понимать, что экзотермический процесс физической адсорбции является обратимым и характеризуется уменьшением энтропии. В процессе физической сорбции никогда не осуществляется распада вещества, фактически отсутствует диссоциация.
Химическая адсорбция
Химическая сорбция – это вид адсорбирования, в результате которой возникает химическое взаимодействие сорбирующей поверхности и адсорбатива. Происходит образование новой ковалентной связи.
Особенность хемосорбции заключается в том, что образуются очень прочные связи. Вещество, подвергшееся хемосорбции сложно убрать с сорбируемой поверхности. Особенность хемосорбции в том, что она высоко специфична, в отличие от физической. Также хемосорбция происходит при более высоких температурах.
Активированная адсорбция
Активированная сорбция — вид сорбции, возникающий за счет реакции между адсорбентом и сорбатом, при котором молекулы адсорбента, провзаимодействовавшие с частицами адсорбата, задерживаются в кристаллической решетке адсорбента. Протекает этот процесс медленно, необратимо и с выделением большого количества теплоты, до нескольких сотен кДж на моль сорбата.
Сравнительная таблица
| абсорбция | адсорбция | |
|---|---|---|
| Определение | Ассимиляция молекулярных частиц в объеме твердого вещества или жидкости называется абсорбцией. | Накопление молекулярных частиц на поверхности, а не в объеме твердого вещества или жидкости, называется адсорбцией. |
| явление | Это массовое явление | Это поверхностное явление. |
| Теплообмен | Эндотермический процесс | Экзотермический процесс |
| температура | Это не зависит от температуры | Благоприятствует низкой температуре |
| Скорость реакции | Это происходит с одинаковой скоростью. | Оно неуклонно увеличивается и достигает равновесия |
| концентрация | Это то же самое по всему материалу. | Концентрация на поверхности адсорбента отличается от концентрации в объеме |
Равновесная адсорбция
Если скорости А. и десорбции равны, то это свидетельствует об установлении адсорбц. равновесия. Кривые зависимости равновесной А. от концентрации или давления адсорбтива при постоянной темп-ре называются изотермами А. Наиболее простая изотерма А. представляет собой прямую, выходящую из начала координат, где на оси абсцисс отложено давление адсорбтива $p$ (или концентрация $c$), по оси ординат – величина адсорбции $a$. Эта область А. называется областью Генри: $a=Γp, Γ$ – коэф. Генри.
И. Ленгмюром была предложена (1914–1918) теория мономолекулярной локализов. А. (молекулы адсорбата не передвигаются по поверхности) при следующих допущениях: поверхность однородна, т. е. все адсорбц. центры имеют одинаковое сродство к молекулам адсорбтива; молекулы адсорбата не взаимодействуют друг с другом. Уравнение Ленгмюра имеет вид: $a=a_{макс}bp/(1+bp)$ или $p=a/b(a_{макс}-a)$, где $a$ – количество адсорбиров. вещества, $a_{макс}$ – предельная величина А. в плотном монослое, $p$ – давление адсорбтива, $b$ – адсорбц. коэф. Полимолекулярная, или многослойная, А., при которой молекулы пара, адсорбируясь, образуют плёнку толщиной в неск. монослоёв, описывается уравнением Брунауэра – Эммета – Теллера (уравнение БЭТ, 1938):$$a=\frac{a_{макс}Cp/p_0}{(1-p/p_0)[1+(C-1)p/p_0},$$где $p_0$ – давление насыщенного пара при темп-ре А., $C$ – константа. Уравнение БЭТ применяют для определения удельной поверхности адсорбентов.
В 1914 М. Полани предложена потенциальная теория А., согласно которой вблизи поверхности адсорбента существует потенциальное адсорбц. поле, убывающее с расстоянием от поверхности; давление адсорбтива, равное вдали от поверхности $p$, вблизи неё возрастает и на некотором расстоянии достигает значения $p_0$, при котором адсорбтив конденсируется.
Адсорбенты обычно разделяют на непористые (радиусы кривизны поверхностей которых весьма велики и стремятся к бесконечности) и пористые. Пористые адсорбенты содержат микро-, супермикро-, мезо- и макропоры (см. Пористость). В макропорах А. крайне мала, её обычно не учитывают при оценке адсорбц. свойств адсорбентов. Характерная особенность А. в микро- и супермикропорах – повышение энергии А. по сравнению с поглощением вещества на непористом адсорбенте той же химич. природы. Этот эффект является результатом наложения полей поверхностных сил противоположных стенок пор. В микро- и супермикропорах А. происходит объёмно, в мезопорах – по механизму послойного заполнения, завершаемого капиллярной конденсацией.
Для микропористых адсорбентов М. М. Дубинин разработал теорию объёмного заполнения микропор (ТОЗМ). Введя представление о функции распределения объёмов пор по значениям химич. потенциала адсорбата в них, Дубинин и Л. В. Радушкевич получили (1947) уравнение изотермы А., которое записывается в виде: $W/W_0=exp[–(A/βE_0)^2]$, где $W$ и $W_0$ – текущая и предельная величины А. пара в единице объёма, $A$ – дифференциальная мольная работа адсорбции, $A=RT\ln(p_0/p)$, $R$ – универсальная газовая постоянная, $T$ – абсолютная темп-ра, $E_0$ – характеристич. энергия адсорбции стандартного пара (обычно бензола или азота), $β$ – коэф. подобия, аппроксимируемый отношением парахоров адсорбируемого и стандартного веществ.
Уравнение Дубинина – Радушкевича применимо для описания изотерм А. в интервале относит. равновесных давлений от 5·10–4 до 0,4 на адсорбентах с однородной микропористой структурой, т. е. адсорбентах, в которых отсутствуют супермикропоры. Т. к. в адсорбц. технике микропористые адсорбенты получили наибольшее распространение, ТОЗМ применяется не только в физико-химич. исследованиях, но и в инженерных расчётах.
Какой из органов выполняет секреторную функцию?
Секреторная функция. Она заключается в выделении пищеварительных соков железами ЖКТ.
Что такое секреторная клетка?
Секреторные нейроны — клетки мозга, специализированные на функции синтеза и секреции биологически активных веществ, например, клетки нейросекреторных ядер гипоталамуса.
Что происходит в петле Генле?
Петля имеет шпилечный изгиб в мозговом слое почки. Главной функцией петли Генле является реабсорбция воды и ионов в обмен на мочевину по противоточному механизму в мозговом слое почки.
Что такое петля Генле?
Петля Генле — часть нефрона, соединяющая проксимальный и дистальный канальцы. Она имеет шпилечный изгиб в мозговом слое почки. Главная функция петли Генле состоит не в реабсорбции воды, а в сохранении ионов в мочевине по противоточному механизму в мозговом слое почки.
Какой процесс происходит в Нефроне?
В нефроне происходят два процесса — фильтрация и обратное всасывание. Фильтрация крови осуществляется в Капсуле Боумена-Шумлянского.
Чем образовано почечное тельце?
Почечное тельце образовано сосудистым клубочком и капсулой. Капсула состоит из 2-х листков – внутреннего и наружного. Сосудистый клубочек состоит примерно из 100 капилляров с фенестрированным и порозным эндотелием. Эндотелиоциты располагаются на внутренней поверхности трехслойной базальной мембраны.
Что входит в состав нефрона?
Нефрон — структурно- функциональная единица почки, состоящая из капиллярного (мальпигиевого) клубочка (5), почечной капсулы (4), в которой происходит фильтрация крови и образование первичной мочи, и извитого канальца (1), в котором происходит реабсорбция — обратное всасывание жидкости из первичной мочи и образование …
Чем представлена паренхима почки?
Кнаружи от пазухи располагается паренхима почки, которая состоит из мозгового и коркового вещества. Корковое вещество, cortes renalis, в виде слоя толщиной 5–7 мм располагается по периферии органа и проникает в виде тяжей – почечных столбов, colunae renalis (Bertini), в толщу мозгового вещества.
Основные различия между абсорбцией и адсорбцией
Поглощение – это процесс, при котором атомы, молекулы или ионы входят в объем
Принимая во внимание, что адсорбция – это накопление молекулярных частиц на поверхности, а не в объеме.
Абсорбция – это эндотермический процесс, тогда как адсорбция – экзотермический процесс.
Абсорбция – это объемное явление, напротив, адсорбция – это поверхностное явление.
Процесс абсорбции остается неизменным во всем материале, тогда как адсорбция – это процесс, который определяется концентрацией веществ.
Процесс абсорбции происходит с одинаковой или равномерной скоростью, с другой стороны, процесс адсорбции вначале быстрый и в конечном итоге замедляется.